
- English
- Español
- Português
- русский
- Français
- 日本語
- Deutsch
- tiếng Việt
- Italiano
- Nederlands
- ภาษาไทย
- Polski
- 한국어
- Svenska
- magyar
- Malay
- বাংলা ভাষার
- Dansk
- Suomi
- हिन्दी
- Pilipino
- Türkçe
- Gaeilge
- العربية
- Indonesia
- Norsk
- تمل
- český
- ελληνικά
- український
- Javanese
- فارسی
- தமிழ்
- తెలుగు
- नेपाली
- Burmese
- български
- ລາວ
- Latine
- Қазақша
- Euskal
- Azərbaycan
- Slovenský jazyk
- Македонски
- Lietuvos
- Eesti Keel
- Română
- Slovenski
- मराठी
- Srpski језик
A BABIO biztosítja az Egyesült Államok FDA 510(k) engedélyét a vírusszállító készletéhez (nem inaktiváló)
A BABIO biztosítja az Egyesült Államok FDA 510(k) engedélyét a vírusszállító készletéhez (nem inaktiváló)
Jinan, Kína – 2025. október – Jinan Babio Biotechnology Co., Ltd. (BABIO)büszkén jelenti be, hogy azBabio® Virus Transport Kit (nem inaktiváló)hivatalosan is megkaptaFDA 510(k) engedély (K250205). Ez a tanúsítvány jelentős mérföldkő a BABIO számára, megerősítve elkötelezettségét a globális minőség, biztonság és innováció mellett a klinikai diagnosztika és a mikrobiológiai szállítási rendszerek terén.
Az FDA 510(k) engedélye engedélyezi a Babio® Virus Transport Kitt mintlényegében egyenértékűaz Egyesült Államokban legálisan forgalmazott eszközökre, igazolva, hogy megfelelnek az Egyesült Államok orvosi eszközökre vonatkozó szabályozási szabványainak. Ez az eredmény bizonyítja a BABIO erős K+F képességeit és gyártási kiválóságát, tovább erősítve globális versenyképességét avírusszállítási és mintagyűjtési piac.
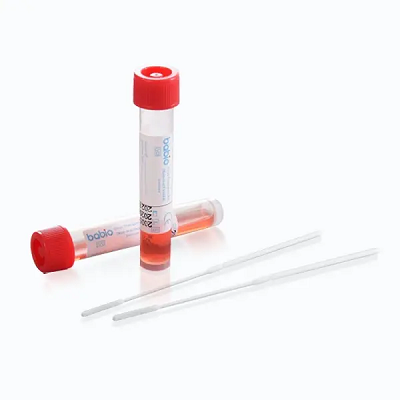
ABabio® Virus Transport Kit (nem inaktiváló)vírusokat tartalmazó klinikai minták gyűjtésére és biztonságos szállítására készült. Fenntartja a minta integritását a későbbi teszteléshez, mint plRT-PCR, víruskultúra, ésmolekuláris diagnosztika, így világszerte alkalmas kórházak, laboratóriumok és közegészségügyi intézmények számára.

BABIO, hogyvezető kínai gyártóA diagnosztikai reagensek, a szállítóközegek és a táptalajok piacán továbbra is növekszik jelenléteEurópa, az Egyesült Államok, Afrika és Délkelet-Ázsia, amely megbízható, nemzetközi szabványoknak megfelelő megoldásokat kínál.
A BABIO tanúsított termékeiről és diagnosztikai innovációiról további információért látogasson el a következő oldalra: https://www.babiocorp.com
#BABIO #FDA510k #Vírusszállítás


